L’organisation de la matériovigilance en Europe et en France est essentielle pour garantir la sécurité des dispositifs médicaux (DM) et assurer une réponse adéquate en cas d’incidents ou de risques.
Cet article vous guidera à travers les acteurs, les responsabilités, et les obligations au sein de ce système.
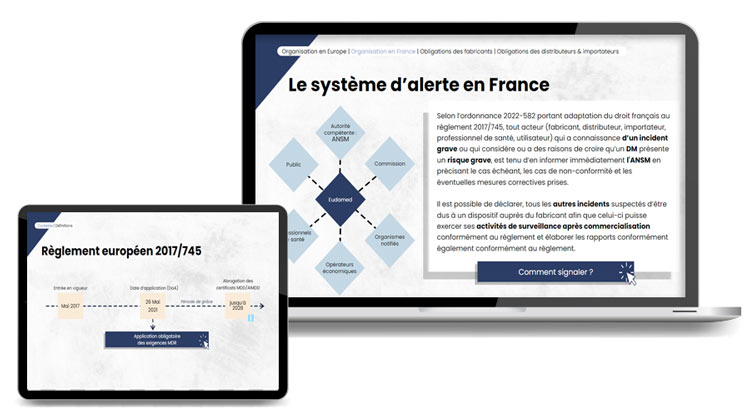
Les acteurs en Europe de la pharmacovigilance
1. Les opérateurs économiques
- Fabricants
- Mandataires
- Distributeurs
- Importateurs
Les opérateurs économiques jouent un rôle clé dans la chaîne de distribution des DM en Europe. Ils sont responsables de veiller à la conformité de ces produits avant leur mise sur le marché.
2. Les utilisateurs
- Les professionnels de santé
- Les utilisateurs de DM
- Les patients
Les utilisateurs jouent un rôle majeur dans la matériovigilance. Ils sont chargés de signaler les incidents et les risques associés aux DM.
3. Les autorités
- La Commission Européenne
- Les États membres de l’UE
- Les autorités compétentes
Les autorités jouent un rôle de supervision et de réglementation. Elles travaillent ensemble pour garantir la sécurité des DM sur le marché européen.
4. Les organismes notifiés
Les organismes notifiés sont responsables de l’évaluation de la conformité de certains produits avant leur mise sur le marché. Ils s’assurent que les DM respectent les normes de sécurité requises.
Les acteurs en France
1. ANSM : Autorité compétente en France pour la matériovigilance
L’Agence Nationale de Sécurité du Médicament et des Produits de santé (ANSM) joue un rôle central dans la matériovigilance en France. Ses responsabilités comprennent :
- Veiller au respect des procédures de surveillance.
- Évaluer et enquêter sur les risques d’incident.
- Prendre des actions correctives de sécurité.
- Communiquer avec la Commission Européenne et les États membres de l’UE sur les mesures prises ou envisagées.
2. Correspondant local
Le correspondant local est un acteur clé dans la matériovigilance en France. Ses missions comprennent :
- Transmettre à l’ANSM les signalements d’incidents ou de risques d’incident.
- Enregistrer, analyser et valider tout incident ou risque d’incident signalé.
- Recommander les mesures à prendre après une déclaration d’incident.
- Conseiller les déclarants pour le signalement des incidents.
- Sensibiliser l’ensemble des utilisateurs aux problèmes de matériovigilance.
- Signaler au centre régional de pharmacovigilance tout incident ou risque provoqué par un DM destiné à l’administration de médicaments.
- Signaler au correspondant local d’hémovigilance si un incident ou risque est en lien avec les produits dérivés du sang.
Obligations des acteurs de la matériovigilance
1. Obligation du fabricant
Le fabricant de DM a plusieurs obligations, notamment :
- Mettre en place un système de surveillance après commercialisation en fonction du niveau du DM.
- Coopérer avec les autorités compétentes sur toutes les mesures prises pour éliminer les risques présentés par des dispositifs.
- Désigner une personne chargée de veiller au respect de la réglementation (PCVRR).
- Sur demande d’une autorité, fournir des échantillons gratuits du dispositif ou donner accès au dispositif.
- Réaliser toute investigation nécessaire.
- Fournir aux autres opérateurs économiques toute information nécessaire pour réaliser l’investigation.
2. Rôle de la PCVRR (Personne chargée de la veille à la réglementation relative aux dispositifs médicaux) dans la matétiovigilance
La personne désignée doit faire en sorte que :
- La conformité des DM soit correctement vérifiée, conformément au système de gestion de la qualité prévu lors de la fabrication.
- La documentation technique et la déclaration de conformité UE soient établies et tenues à jour.
- Les obligations en matière de surveillance et de notification de matériovigilance après commercialisation soient remplies.
- La déclaration nécessaire pour l’objet d’une investigation soit délivrée.
3. Obligation du distributeur et importateur
Les distributeurs et les importateurs de DM ont également des obligations, notamment :
- Avoir un registre des réclamations des dispositifs non conformes, des rappels et retraits.
- Fournir aux autres opérateurs économiques toute information nécessaire pour réaliser l’investigation.
- Coopérer avec les autorités compétentes sur toutes les mesures prises pour éliminer les risques présentés par des dispositifs.
- Sur demande d’une autorité compétente, fournir des échantillons gratuits du dispositif ou donner accès au dispositif.
- Avoir des conditions de stockage et de transport adaptées et conformes.
Conclusion
En conclusion, la matériovigilance joue un rôle fondamental dans la garantie de la sécurité des dispositifs médicaux en Europe et en France. Les différents acteurs, qu’il s’agisse des fabricants, des utilisateurs, des autorités ou des organismes notifiés, contribuent activement à la surveillance et à la gestion des incidents et des risques liés à ces dispositifs. Cela permet d’assurer la protection des patients et d’élever les normes de qualité des soins de santé.
Il est primordial que tous les acteurs comprennent et respectent leurs obligations en matière de matériovigilance, car cela a un impact direct sur la sécurité des patients et la confiance dans les dispositifs médicaux.
L’importance de la formation
Si vous êtes impliqué dans l’industrie des dispositifs médicaux ou si vous cherchez à approfondir vos connaissances sur la matériovigilance, nous vous encourageons à explorer la formation en ligne sur la matériovigilance. Cette formation en e-learning vous permettra de mieux comprendre les enjeux de la matériovigilance, les responsabilités des acteurs, et les meilleures pratiques pour garantir la sécurité des dispositifs médicaux. C’est une opportunité précieuse pour renforcer vos compétences et contribuer à la sécurité des patients.
Pour en savoir plus sur cette formation, veuillez visiter le lien suivant : Formation en ligne sur la Matériovigilance. Investir dans votre formation et votre compréhension de la matériovigilance est un pas important vers un secteur des dispositifs médicaux plus sûr et plus fiable.
Foire aux questions
Qu'est-ce que la matériovigilance et pourquoi est-elle importante en France et en Europe ?
La matériovigilance est un système de surveillance des dispositifs médicaux visant à assurer leur sécurité. Elle est essentielle pour protéger les patients et garantir la qualité des soins de santé en France et en Europe.
Qui sont les acteurs clés de la matériovigilance en Europe ?
Les acteurs clés de la matériovigilance en Europe comprennent les opérateurs économiques, les utilisateurs, les autorités et les organismes notifiés.
Quelles sont les obligations des fabricants de dispositifs médicaux en matière de matériovigilance ?
Les fabricants doivent mettre en place un système de surveillance après commercialisation, coopérer avec les autorités compétentes, désigner une personne chargée de veiller au respect de la réglementation, fournir des échantillons gratuits sur demande, réaliser des investigations, et fournir des informations aux autres acteurs.
Quel rôle joue la PCVRR dans la matériovigilance ?
La PCVRR veille à la conformité des dispositifs médicaux, à la documentation technique, aux obligations de surveillance et de notification, et à la délivrance des déclarations nécessaires pour les investigations.
Avantages des formations e-learning
L’e-learning offre de nombreux avantages pour les apprenants, tels que la flexibilité, l’accessibilité et la possibilité de revenir sur des points importants à tout moment. Les formations en ligne proposent également des outils interactifs, tels que des quiz d’évaluation, pour vérifier les connaissances acquises et obtenir une attestation d’assiduité.
Afin que tous les acteurs de l’industrie de la santé, en particulier ceux liés aux dispositifs médicaux tels que les start-ups et les agences d’intérim, puissent connaître leurs responsabilités et les règles de la matériovigilance associées à leur secteur d’activité.

Eric Villemagne, Directeur Général chez IFIS Interactive depuis plus de 10 ans, incarne avec excellence l’expertise et l’innovation dans le domaine de la formation e-learning pour les industries de santé. Fort d’une ancienneté de plus de 20 ans au sein du groupe IFIS et d’une expérience enrichissante de 25 ans dans le secteur de la formation, sa carrière est marquée par une contribution significative à l’évolution et à l’amélioration des processus d’apprentissage. Diplômé d’un Executive MBA de l’EM Lyon, Eric s’engage avec détermination à fournir des formations sur étagère et sur mesure, répondant précisément aux besoins des professionnels de l’industrie pharmaceutique, du dispositif médical et de la cosmétique.
Sa vision stratégique ne s’arrête pas là. Eric ambitionne de contribuer activement à la relocalisation et au développement durable de ces industries cruciales en France et en Europe. Par ce biais, il affirme non seulement son leadership mais également son engagement indéfectible envers l’excellence éducative et industrielle. Sa démarche vise à instaurer un environnement propice à l’innovation et à la croissance durable, en mettant l’accent sur des solutions de formation qui anticipent et répondent aux défis de demain.



